Radioterapia pulsada de rayos X
Sumario:
Hoy en día el cáncer es la segunda causa de muerte en los países desarrollados, y se espera que sea la principal antes de que termine este siglo. Sin embargo a pesar de este desolador panorama a lo largo de estas últimas décadas se ha producido un espectacular aumento en la supervivencia media de los […]
Hoy en día el cáncer es la segunda causa de muerte en los países desarrollados, y se espera que sea la principal antes de que termine este siglo. Sin embargo a pesar de este desolador panorama a lo largo de estas últimas décadas se ha producido un espectacular aumento en la supervivencia media de los pacientes diagnosticados con tan terrible enfermedad. El desarrollo de técnicas de radioterapia y quimioterapia, cada vez más específicas y eficaces, nos hace albergar la esperanza de que en un futuro no muy lejano la mortalidad asociada a ciertos tipos de cáncer disminuirá muy significativamente.
Restringiéndonos a las técnicas de radioterapia, una vez identificado y localizado el tumor, éste se irradia con radiación ionizante –por ejemplo rayos X, electrones o protones- con el objetivo de dañar el ADN de las células tumorales induciendo su muerte celular. Aunque, como decíamos antes, los tratamientos son cada vez más refinados, es inevitable la presencia de indeseables efectos secundarios. Por ejemplo el tejido sano que rodea al tumor también se ve irradiado, aunque estas células sanas son capaces de reparar el daño en el ADN de una forma mucho más eficiente si la dosis se administra de forma fraccionada.
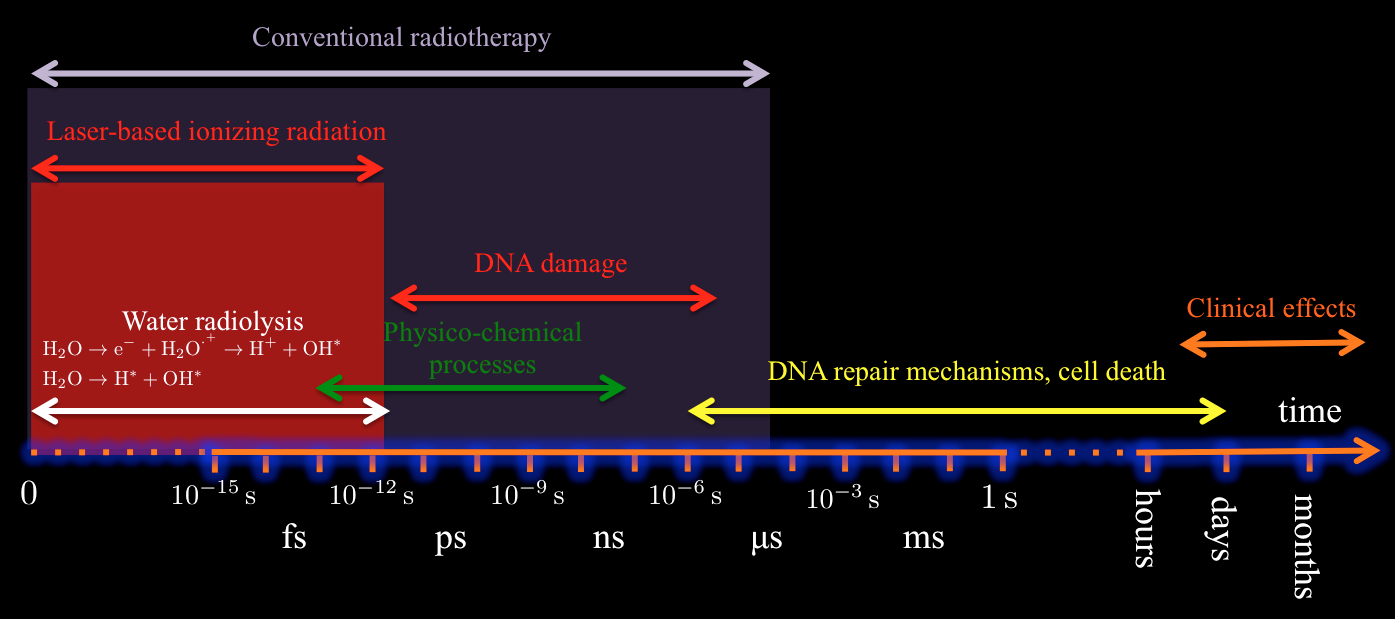
También es muy interesante analizar la forma en el que la dosis se deposita en el tejido tumoral. En la actualidad, las técnicas de radioterapia convencionales emplean fuentes pulsadas de radiación ionizante (con pulsos de microsegundos y espaciados milisegundos) siendo las dosis típicas por fracción de unos dos grays (un gray es un julio de energía de radiación absorbida por un kilogramo de la materia), siendo esta energía distribuida sobre un intervalo de tiempo relativamente grande (del orden de minutos).
Este enfoque presenta en principio varias desventajas claras. Uno de los aspectos que sería deseable mejorar en los tratamientos de radioterapia actuales es el tiempo de exposición del paciente. Al depositarse la dosis en un periodo extenso de tiempo, se obliga al paciente a permanecer lo más inmóvil posible a fin de evitar incertidumbres dinámicas de posición y anatomía -es decir para evitar irradiar tejido sano-. También en el contexto de tiempos largos de tratamiento es muy interesante analizar el efecto de una deposición de energía pulsada pero con pulsos relativamente largos, del orden de microsegundos, con el consiguiente daño biomolecular en la membrana y el ADN, y su solapamiento temporal con los mecanismos de reparación celular. ¿Se ven estos afectados? ¿Se puede complicar los procesos biológicos implicados en la reparación del ADN del tejido sano circundante? ¿Sería más beneficioso no solapar temporalmente la irradiación y los mecanismos de reparación celular? ¿A tasas muchos más altas de irradiación que las que actualmente tenemos se podrían inducir efectos no lineales? ¿Se podrían acumular efectos subletales y convertirlos en letales?

Estas preguntas cobran especial relevancia en estos últimos años ya que el desarrollo constante de la tecnología láser, y un mayor conocimiento de los mecanismos de interacción láser-materia a altas intensidades, nos han proporcionado fuentes pulsadas de radiación ionizante con una duración de decenas de femtosegundos con unos flujos instantáneos muy relevantes. Para entender el nuevo escenario que se abre es necesario comprender que 1 segundo son 1.000.000.000.000.000 femtosegundos, siendo los periodos vibracionales de los núcleos en una molécula del orden de decenas de femtosegundos. En otras palabras, cuando un pulso tan corto temporalmente interacciona con la materia ésta está “congelada”. Sólo permanece el movimiento de los electrones que tiene lugar en la escala de los atosegundos.
Al irradiar un tejido tumoral con pulsos de rayos X de flujo instantáneos muchísimo más altos que los que manejamos hoy en día, es de esperar que los efectos no lineales de interacción de la radiación con la materia empiecen a jugar un papel relevante. Por ejemplo se podría pensar en inducir la acumulación de eventos subletales, eventos típicos radiaciones de baja LET -Linear Energy Transfer- como fotones y electrones, hasta convertirlos en letales produciendo por tanto la muerte celular. Si esta hipótesis fuera cierta, observaríamos cómo la supervivencia celular incluso para radiaciones de baja LET decrece linealmente con la tasa de dosis si el flujo instantáneo es lo suficientemente elevado.
Otro aspecto muy interesante de este tipo de fuentes ultracortas es la posibilidad de estudiar los mecanismos de reparación celular desde sus primeros estadios. En un sentido amplio, podemos hablar de mecanismos de reparación desde el momento en que las moléculas irradiadas intentan «desembarazarse» del exceso de energía que hemos aportado. A un nivel molecular, estos mecanismos empiezan a los pocos femtosegundos después de la irradiación pudiéndose inducir por ejemplo la fotofragmentación de la molécula, la excitación de ciertos modos específicos de vibración molecular que nos resulten interesantes, o cambios conformacionales. No es descabellado pensar que un conocimiento de la dinámica de relajación celular a un nivel tan detallado nos puede proveer de nuevas estrategias de radioterapia más eficientes que las actuales.
A día de hoy nadie tiene claro nada en este campo. Parece que existen ciertos indicios que muestran que un tratamiento de radioterapia con pulsos ultracortos podría presentar ciertas ventajas sobre las técnicas de radioterapia convencional, pero los resultados no son concluyentes.
Para poder responder a los interrogantes que deja este artículo sólo nos queda trabajar duro entre todos. Trabajar combinando expertos en biología celular, biomedicina, tecnología láser, e interacción láser-materia. El camino parece prometedor.






