Nuestra particular deuda con Hiroshima y Nagasaki (parte 2)
Sumario:
En esta segunda parte del post se describen los efectos, agudos y tardíos, que, como consecuencia de su exposición a la radiación, sufrieron y aun sufren las víctimas de los bombardeos y que han sido cuantificados en todos los estudios epidemiológicos realizados sobre los supervivientes (el Life Span Study, LSS). Entre estas víctimas están incluidas, […]
En esta segunda parte del post se describen los efectos, agudos y tardíos, que, como consecuencia de su exposición a la radiación, sufrieron y aun sufren las víctimas de los bombardeos y que han sido cuantificados en todos los estudios epidemiológicos realizados sobre los supervivientes (el Life Span Study, LSS). Entre estas víctimas están incluidas, por supuesto, aquellos aun no nacidos que se encontraban en el vientre materno en el momento de las explosiones (irradiados in-utero). También veremos qué dice el estudio epidemiológico sobre los efectos hereditarios en los descendientes de aquellas víctimas.
Antes de continuar, hagamos un pequeño recordatorio de cómo la radiación daña las células y qué tipos de efectos celulares podrán producirse a consecuencia de ese daño. De la naturaleza de estos dependerán los efectos tisulares y orgánicos y, en última instancia, los daños en el individuo y su descendencia.
La ionización del medio intracelular producida por la radiación puede inducir cambios en el ADN que ponen en marcha de forma inmediata los mecanismos de reparación celular, los cuales deberán actuar antes de que la célula progrese hasta la mitosis. En ese momento la célula tendrá tres posibles “opciones”:
- El ADN puede haber sido completa y correctamente reparado y la célula y su descendencia mantendrán todas sus funciones intactas.
- Otra posibilidad es que la reparación no tenga éxito y los mecanismos de control del ciclo celular detecten ese código genético defectuoso y respondan provocando la muerte de la célula, mediante la apoptosis o alguna otra forma de suicidio celular o muerte celular activa (necroptosis, autolisis y otros), que son, en general, las vías más comunes de muerte celular, tanto en desarrollo normal como en respuesta a un daño externo (la forma en que se producen, la preferencia por una u otra forma… todo este asunto del suicidio celular merece un post por si solo). Es también posible que los mecanismos de control no activen estos procesos y la célula continúe su ciclo, pero el daño del ADN sea incompatible con una correcta mitosis. En este caso la célula sufrirá, muy probablemente, una catástrofe mitótica y muera durante la mitosis. La catástrofe mitótica es un mecanismo de muerte muy frecuente en respuesta a la irradiación. Puede ocurrir también que esos daños permitan a la célula replicarse correctamente pero acaben, tras algunos ciclos reproductivos, derivando en una muerte clonogénica o reproductiva, en cuyo caso toda la estirpe descendiente de aquella célula terminará perdiendo su capacidad proliferativa, lo que equivale a la muerte. Todas estas formas de respuesta concluyen por tanto de la misma manera, con la muerte o incapacidad reproductiva de la célula o su descendencia.
- La tercera posibilidad es que la reparación, aun no siendo perfecta, resulte en una alteración en el ADN compatible con la continuidad del ciclo reproductivo. Esa mutación no supondrá, en la inmensa mayoría de casos, ningún perjuicio ni ventaja significativos y la célula podrá mantener su capacidad proliferativa. Pero la posibilidad más grave, aunque remota, será que esa mutación provoque cambios drásticos de los mecanismos de control del ciclo celular que podrían colaborar con un proceso carcinogénico o, incluso, iniciarlo.
Los efectos agudos de la irradiación
La muerte de una única célula en un organismo maduro no tendrá, en genreal, consecuencias, pues los tejidos están formados por un número muy grande de ellas. Ni siquiera la muerte de un número pequeño de células (con algunas excepciones). Para que tenga consecuencias clínicas en el individuo debe producirse la muerte de un número suficientemente grande de células para provocar el fallo del órgano o tejido correspondiente, y ello requiere que tanto la dosis como el volumen irradiado sean grandes. Solo dosis mayores que un valor determinado, que llamamos dosis umbral, podrán provocar un determinado efecto. Solo para dosis mayores que este umbral el efecto aparecerá y lo hará con seguridad, por lo que se les denomina efectos deterministas. Obviamente, el efecto será más grave cuanto mayor sea la dosis o el volumen irradiado, pues mayor será el número de células muertas. Entre los efectos deterministas asociados a la muerte celular en organismos maduros tenemos todos los efectos agudos de la radiación.
La irradiación del cuerpo completo con dosis moderadas (a partir de aproximadamente 1 Gy o incluso menos) provoca una serie de síntomas que se manifiestan agrupados en lo que conocemos como síndrome de irradiación aguda.
Hay que tener en cuenta que la información recopilada sobre la respuesta aguda en la población bombardeada fue escasa. Las precarias condiciones en las que se realizó la atención a los heridos, junto a la gravedad de los daños no radiológicos, exacerbaron los efectos de la radiación, lo que limitó mucho la información obtenida y la hizo difícilmente extrapolable. Este artículo (que ya mencioné en la primera parte del post) resume los efectos agudos observados en las víctimas y todos los problemas relacionados con su registro y tratamiento.
Sobre la evolución clínica del síndrome agudo de irradiación y su tratamiento médico, especialmente a dosis más altas, tenemos también datos procedentes de otros accidentes, principalmente de Chernobyl, al que dediqué este post.
La siguiente tabla resume los síntomas agudos de la irradiación, su tiempo hasta la manifestación y la incidencia, para cada intervalo de dosis absorbidas en cuerpo completo.
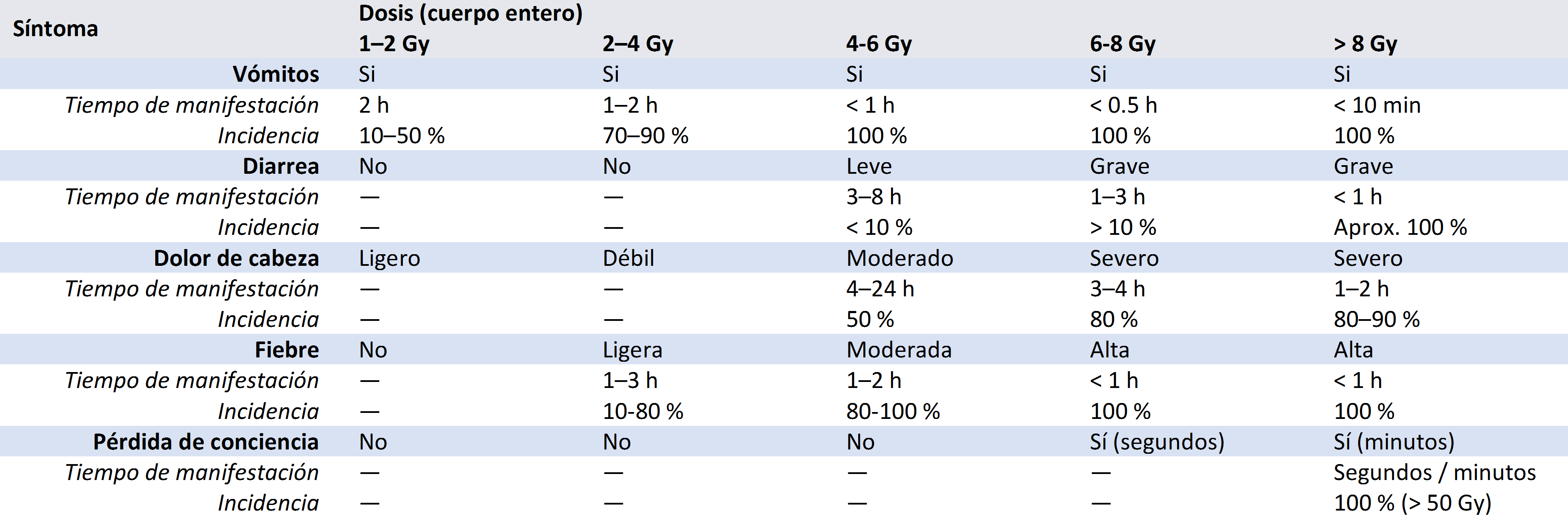
Se distinguen, por convención, tres subsíndromes :
- Hematopoyético, iniciado por la muerte de las células madre pluripotenciales de la médula ósea que causará anemia, leucopenia y plaquetopenia que pueden derivar en infección, fiebre y hemorragias (subdérmicas, lo que se conoce como púrpura, o internas), especialmente en presencia de heridas por otras causa, como fue el caso,
- Gastrointestinal, producido por daños en las células basales de la mucosas intestinal que derivarán en nauseas, vómitos y dolor abdominal y una posterior pérdida de electrolitos por la reducción de la capacidad de absorción intestinal.
- Neurovascular, posiblemente producido por la inflamación resultante del daño en los tejidos endotelial y vascular que produciría un aumento de la presión intracraneal (aunque el mecanismo exacto no es aun bien conocido), y que se manifiesta con mareo, dolor de cabeza e incluso la pérdida de conciencia.
El síndrome de radiación aguda puede llegar a provocar, incluso en el intervalo de dosis más bajas (1-2 Gy), la muerte de la persona irradiada en pocos días o semanas y la probabilidad de que la muerte ocurra, así como el tiempo que haya de transcurrir para que ocurra, dependerá de la dosis absorbida, de si existen lesiones de otra naturaleza y de si la persona recibe o no tratamiento médico adecuado.
En Hiroshima y Nagasaki las personas que recibieron dosis superiores a 1 Gy sufrieron daños severos de otra naturaleza y recibieron un tratamiento médico insuficiente (por carencia de medios y por desconocimiento, pues era la primera vez que el ser humano se enfrentaba a los daños por radiación), lo que elevó la mortalidad por síndrome de irradiación en todos los intervalos de dosis.

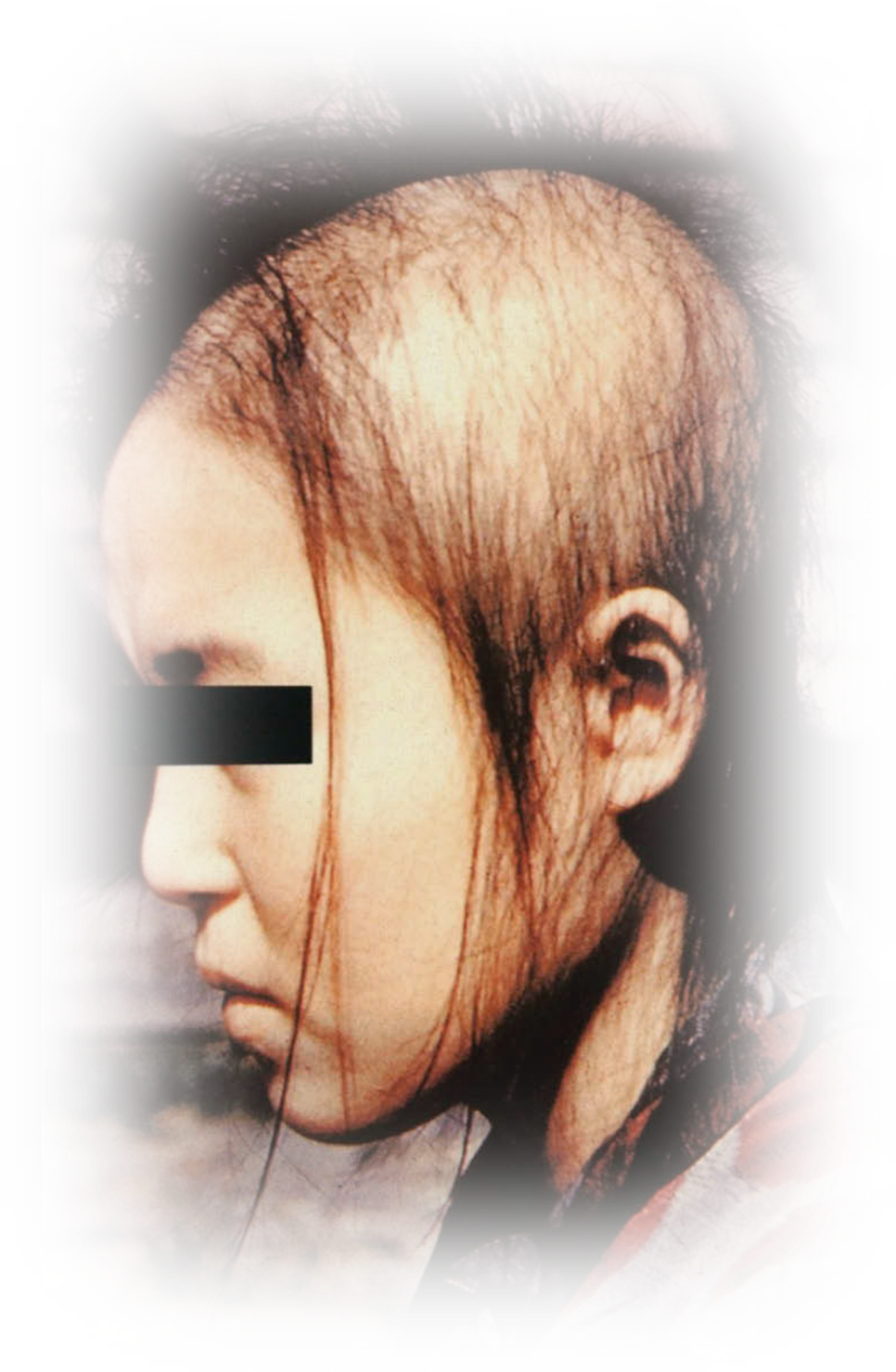
de Nagasaki.
El síndrome de irradiación aglutina los efectos agudos y deterministas más severos, pero no son los únicos.
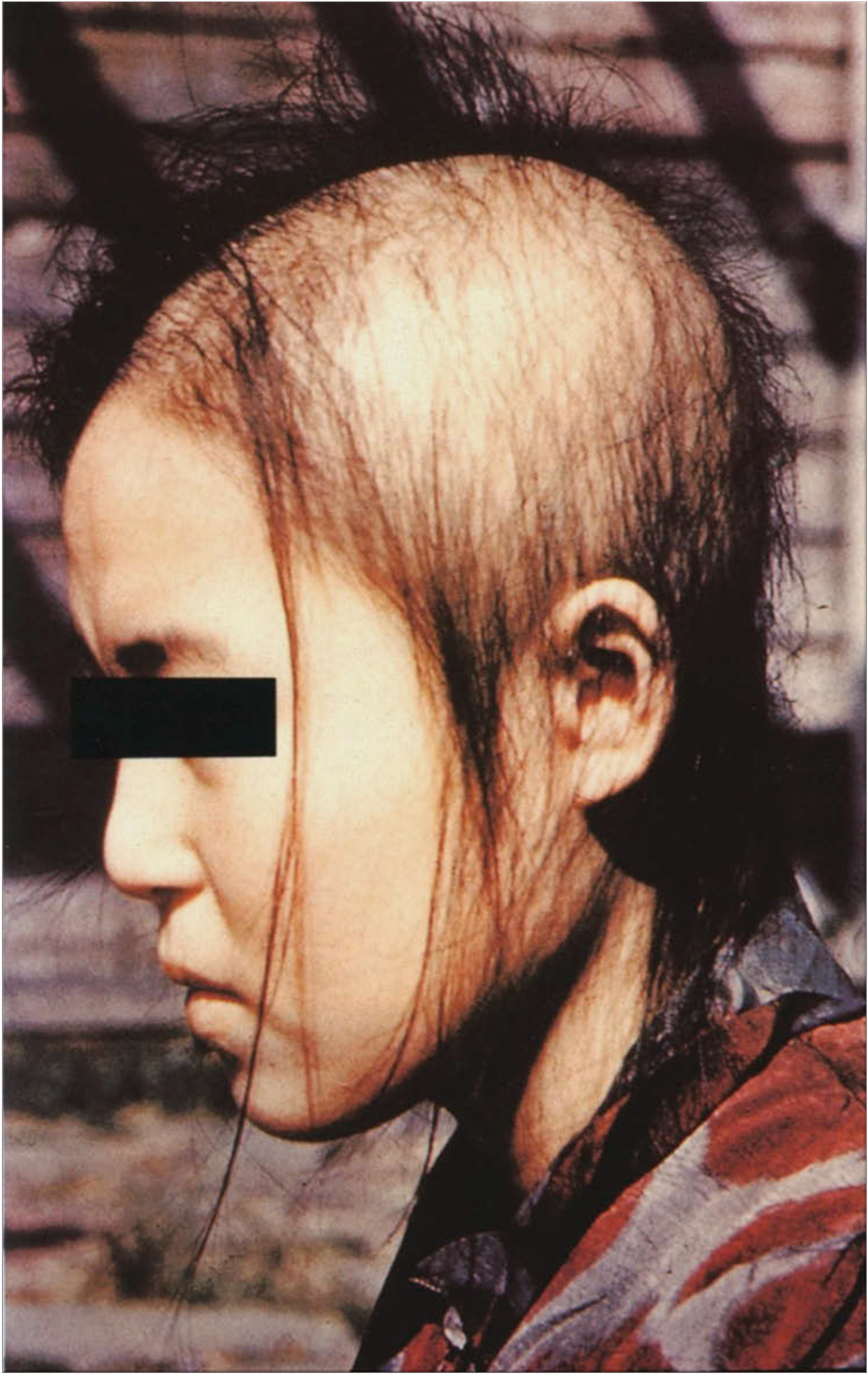
Otro efecto agudo característico de la irradiación, que se presenta también a dosis muy bajas, es la alopecia. El mecanismo por el que ocurre tampoco es bien conocido, pero se cree que la muerte de unas pocas células del folículo piloso es suficiente para producir una reducción en el grosor y calidad estructural del cabello que resultan en una extrema fragilidad. La siguiente figura representa la probabilidad de alopecia en función de la dosis en cuero cabelludo, entre las víctimas de los bombardeos.
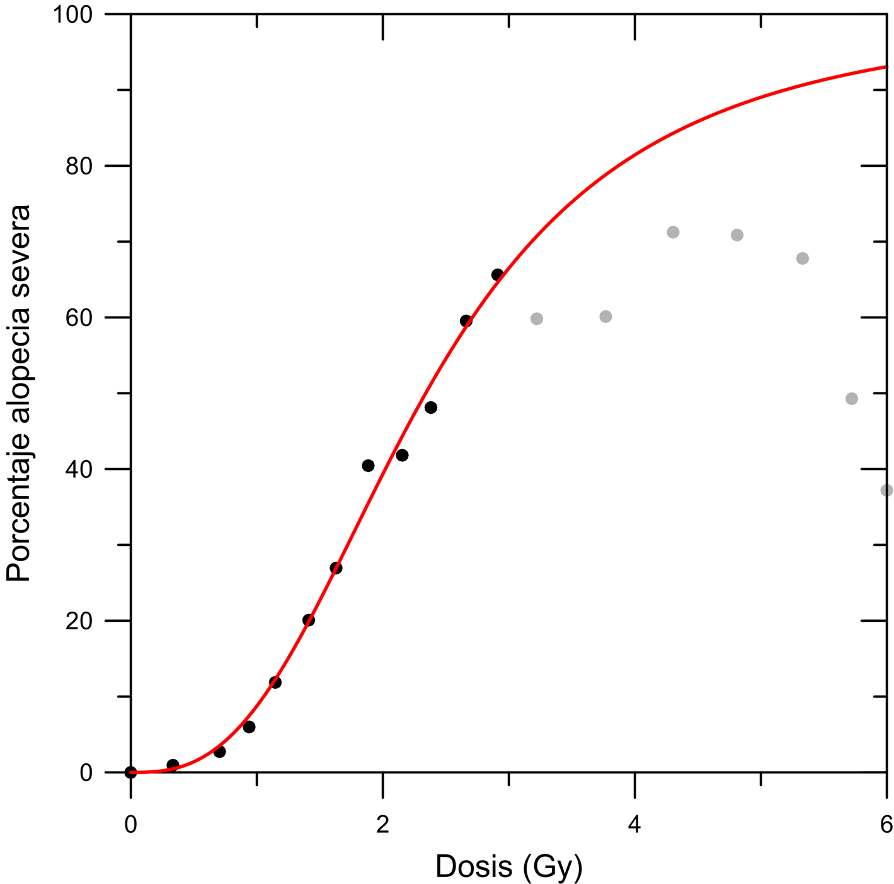
Los efectos a largo plazo de la radiación
A diferencia de la muerte celular, una mutación maligna puede suponer una amenaza para la vida de un individuo aun cuando solo aparezca en una única célula. El desarrollo de un cáncer a partir de esa mutación es un proceso de degradación celular por etapas que abarcará al menos algunos años hasta su manifestación clínica y su diagnóstico. Se trata por ello de un efecto tardío cuya investigación precisa un seguimiento de largo plazo.
Bajo el paradigma vigente, el efecto carcinogénico de la radiación es visto como un proceso absolutamente estocástico (azaroso) que puede ocurrir incluso para dosis extremadamente bajas, lo que significa que no existe un umbral seguro de dosis por debajo del cual podamos tener garantía de que el efecto no aparecerá. Por decirlo de forma visual, una única partícula ionizante puede provocar, en una única célula, una mutación que inicie un proceso carcinogénico. Este paradigma, que se conoce como modelo lineal sin umbral y había sido ya planteado en la primera mitad del siglo XX, se sostiene principalmente en la evidencia surgida del seguimiento de la población de Hiroshima y Nagasaki.
Realmente, el cáncer requiere la activación de un gran número de mutaciones relacionadas con múltiples funciones celulares. Pero hoy aceptamos que algunas mutaciones especialmente graves tienen un papel muy relevante en el proceso al facilitar la consecutiva acumulación de mutaciones adicionales, y que la radiación es un agente especialmente capaz de producir este tipo de mutaciones.
Respecto a la carcinogénesis, el seguimiento de los supervivientes de los bombardeos arroja evidencia suficiente: la radiación incrementó la incidencia de cáncer, y sigue incrementándola. Todo el mundo tiene idea de ello. Pero ¿cómo de importante es ese incremento?. La siguiente figura lo ilustra de forma suficientemente clara para la incidencia de cáncer sólido y leucemia.
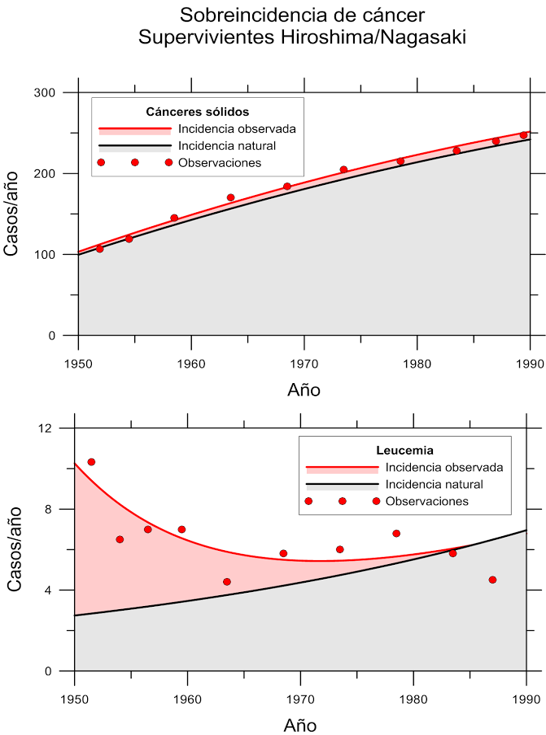
En resumen, el bombardeo ha incrementado, hasta el momento, en un 11 % la incidencia de los cánceres sólidos y en un 46 % la de todas las formas de leucemia y linfoma agudos. Dicho en números absolutos, entre los 86700 individuos irradiados con dosis superiores a 5 mGy que se incluyeron en el LSS, se han diagnosticado, hasta 2015, 7851 casos, frente a los 7000 que habrían sido diagnosticados en una población no irradiada. Solo 850 casos de cáncer atribuibles a la radiación de los bombardeos. Es un incremento considerable, sin duda, pero muy alejado del valor que, según mi experiencia, ha calado entre la opinión pública. Los números para leucemias y linfomas son aun más sorprendentes, dada la baja incidencia natural. Así, donde se esperaban unos 111 casos (con una importante incertidumbre), se ha observado un exceso de unos 94 casos, hasta contabilizar los 204 (en 2015). La leucemia es un tipo de cáncer de aparición aguda, con tiempo de latencia muy corto, por lo que ese incremento tuvo lugar en los 30 años después de las explosiones y hoy día la incidencia anual en la población bombardeada coincide con la que habría habido sin los bombardeos.
No muestra el LSS relación con la radiación para la leucemia linfocítica crónica, pero el análisis a largo plazo de la cohorte de liquidadores de Chernobyl indica que también esta forma de leucemia puede ser producida por la radiación.
Por supuesto, la probabilidad de sufrir un cáncer radioinducido aumenta al aumentar la dosis recibida. El LSS muestra que esta dependencia se ajusta bien al modelo lineal sin umbral, al menos en el rango de dosis al que la población de Hiroshima y Nagasaki estuvo expuesta y con las incertidumbres, considerables, del estudio.
La figura siguiente muestra esta proporcionalidad para la población de Hiroshima y Nagasaki (puntos negros) y la obtenida del estudio INWORKS (puntos rojos). La coincidencia entre ambas poblaciones es muy buena, a pesar de que en el caso de INWORKS las dosis absorbidas, muy bajas, fueron el resultado, no de una exposición aguda, como en la población bombardeada, sino de una exposición ocupacional crónica a lo largo de muchos años.
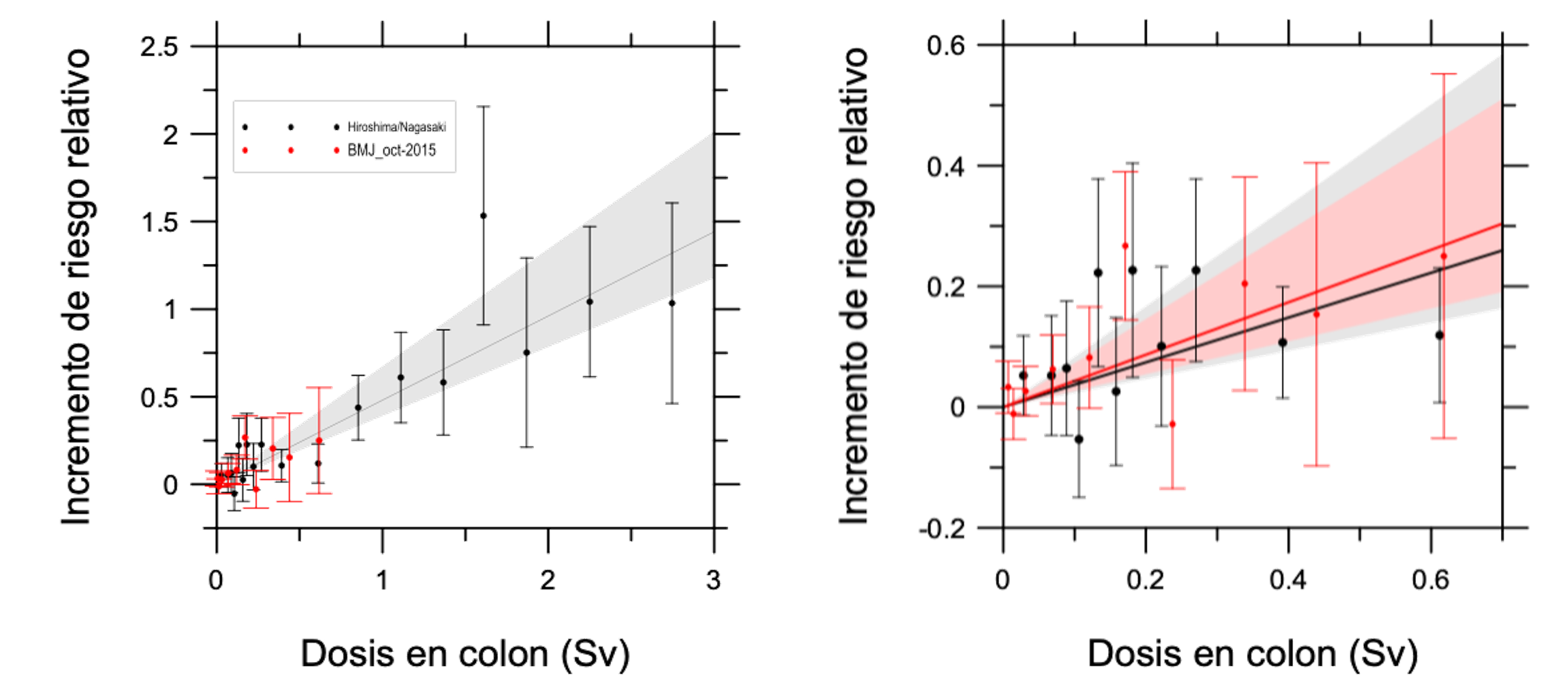
Este es el modelo de dosis-riesgo aceptado hoy y que difícilmente podremos desterrar (al menos en un futuro inmediato), dada la dificultad de realizar un estudio que no esté afectado por tremendas incertidumbres dosimétricas y epidemiológicas para las dosis muy bajas. Y ha sido este modelo, surgido del sufrimiento de aquellas víctimas, el que ha impulsado en las últimas décadas la técnica y la ciencia radiológica hasta unos niveles de seguridad superiores a los de la mayoría de actividades humanas.
Los datos epidemiológicos del LSS nos han permitido también estimar la propensión de cada tejido a desarrollar un cáncer radioinducido, e incluso distinguir (al límite de la significación estadística) un nivel de riesgo diferente para mujeres y hombres (el valor adoptado en el modelo es el promedio de ambos sexos).
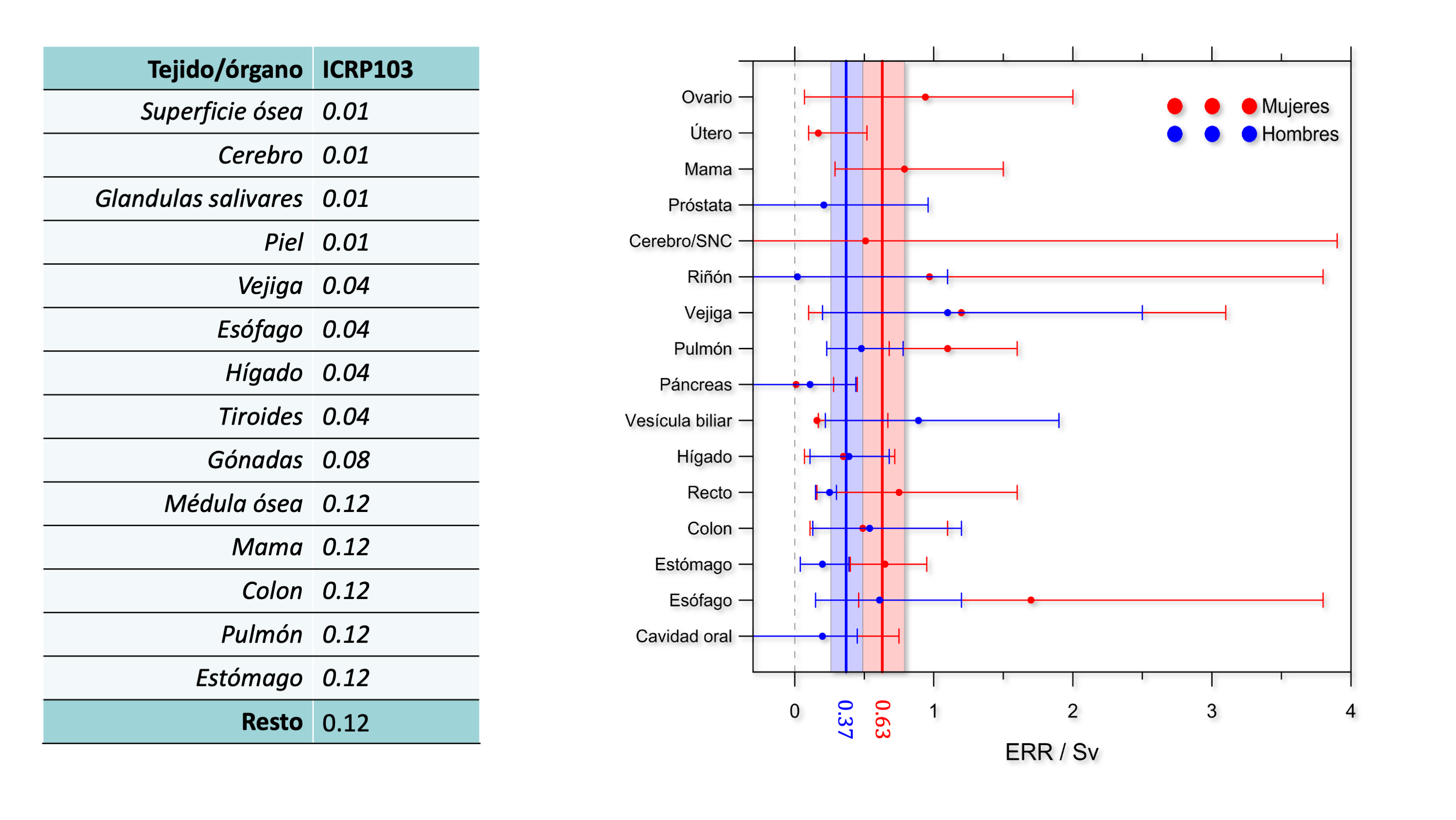
No todo es cáncer. Otros efectos a largo plazo.
El estudio a largo plazo de los supervivientes ha evidenciado también la mayor incidencia de otras patologías, no neoplásicas, relacionadas con la irradiación.
El más conocido de estos efectos no agudos es la catarata. Esta apareció en general tras un periodo de latencia de entre dos y diez años (si bien algunos casos se manifestaron tras solo tres meses) y generalmente como catarata posterior subcapsular y catarata cortical, formas títpicamente asociadas a la irradiación. Los datos del LSS muestran que la dosis umbral para este efecto, si la hay, es menor de 1 Gy. El mecanismo por el cual la catarata, que es un efecto deterministas, se forma incluso a dosis tan bajas es complejo y está relacionado con la particular organización encapsulada de ese órgano.
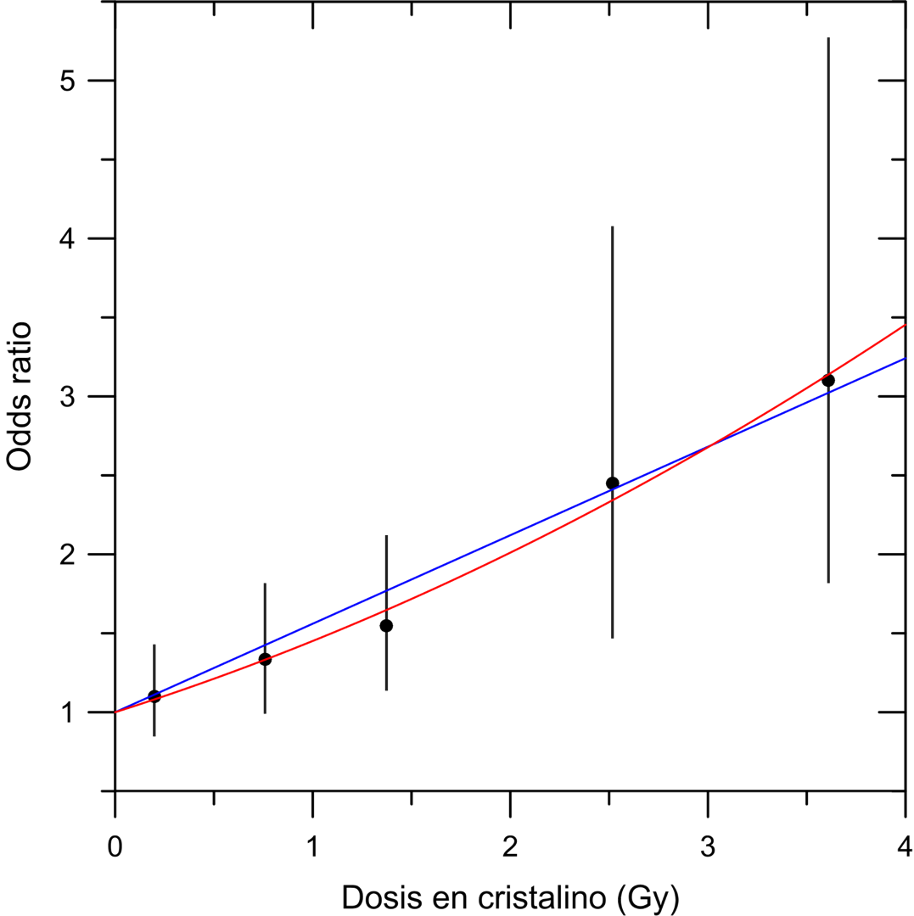
Además de la catarata, otras patologías se han manifestado a más largo plazo en la población irradiada. Los mecanismos por los que algunas de estas aparecen no están claros, pero podrían estar relacionados con la respuesta aguda inflamatoria o el deterioro inmunológico derivado de la aplasia medular. Uno de los que más interés despierta, y que se ha visto confirmado en el seguimiento de los liquidadores de Chernobyl, es el infarto de miocardio. También el ictus cerebral muestra coeficientes de riesgo muy significativos. Estos efectos muy tardíos presentan umbrales de dosis muy bajos o inexistentes.
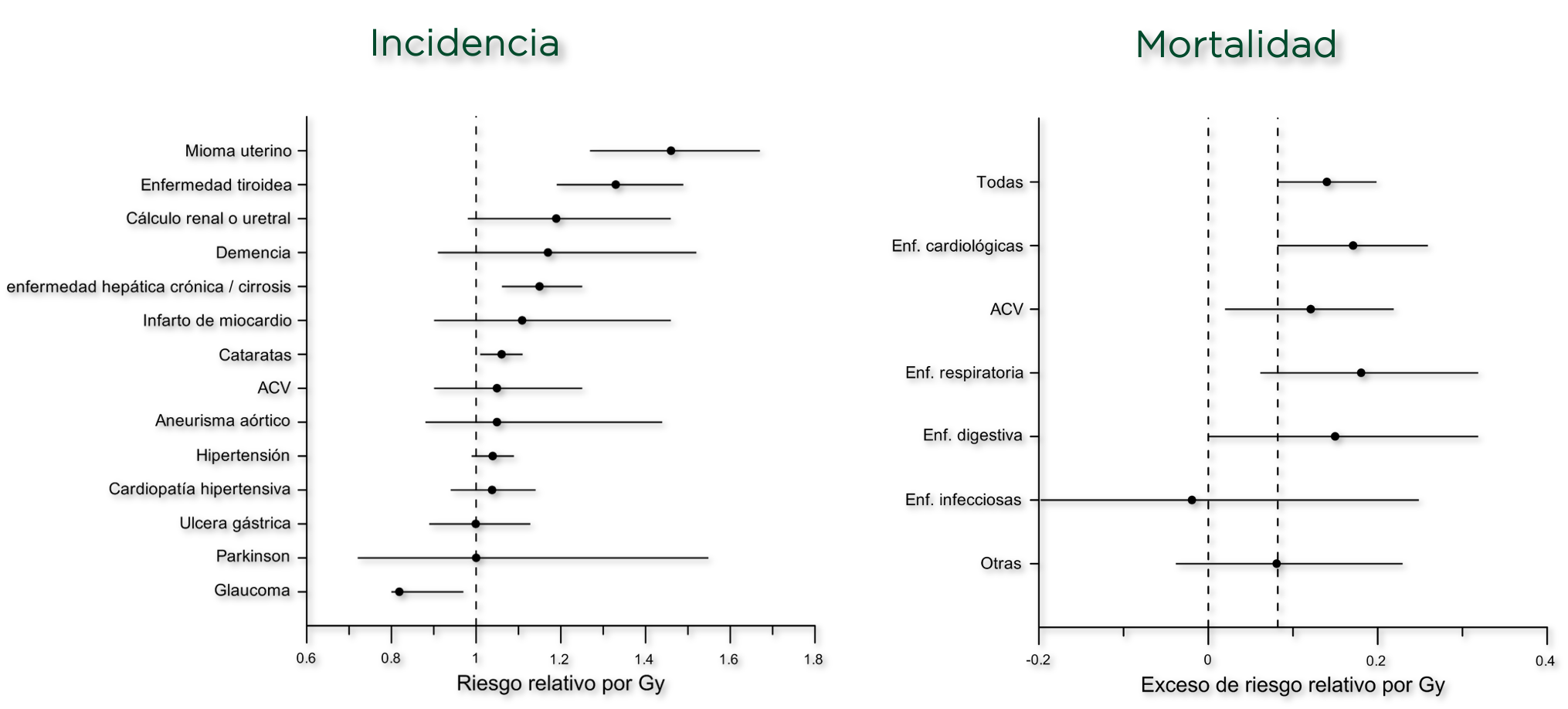
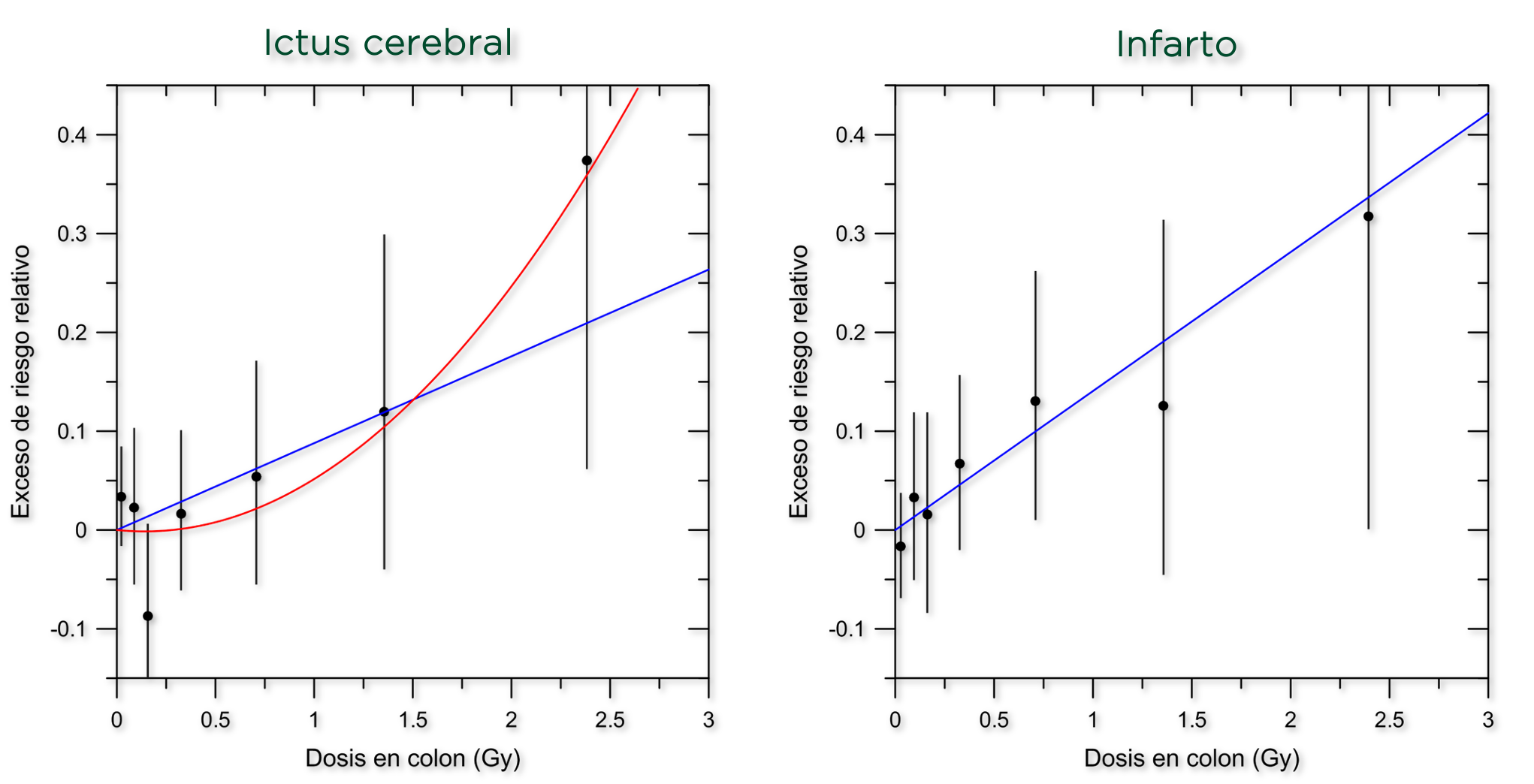
Solo un estudio como el LSS, con seguimientos a tan largo plazo de una población considerable cuyo nivel de exposición puede conocerse con una precisión aceptable, ha podido aportar la evidencia de la existencia de estos efectos que de otra forma serían imposibles de observar.
Irradiados in-utero: efectos en el embrión
Los efectos en el embrión pueden estar asociados a la muerte celular o a la mutación carcinogénica. Tres son los efectos observados:
- La muerte de incluso unas pocas células en un embrión en las primeras etapas del desarrollo, que puede resultar en su inviabilidad y en un aborto espontáneo.
- La muerte de un número pequeño de células durante la etapa de organogénesis (semanas 3ª a 8ª) o durante el desarrollo del córtex (semanas 8ª a 25ª), que puede provocar malformaciones y retraso mental.
- La mutación oncogénica en los tejidos del embrión, especialmente en la última etapa, que aumentará el riesgo de cáncer a lo largo de su vida.
Los tres efectos se han estudiado en la población expuesta in-útero en Hiroshima y Nagasaki y los resultados contradicen las ideas comunes que se tienen sobre el asunto.
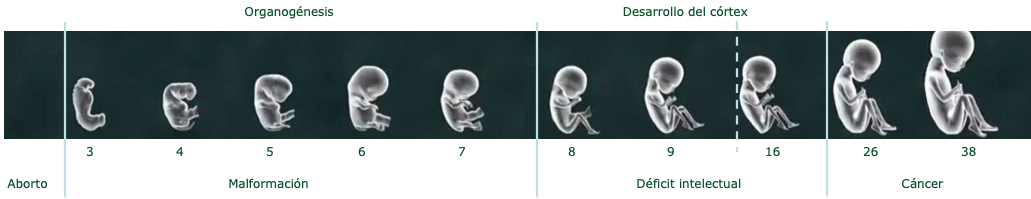
La incidencia de abortos y malformaciones en el grupo de personas irradiadas in-utero en Hiroshima y Nagasaki no muestra diferencia estadísticamente significativa respecto a la que cabría esperar en una población no irradiada.
Respecto al retraso mental, los datos de Hiroshima y Nagasaki sí muestran un claro impacto de las dosis recibidas in-utero, pero solo en aquellos que fueron irradiados entre las semanas 8ª a 26ª de desarrollo y con dosis más altas (> 0.5 Gy).
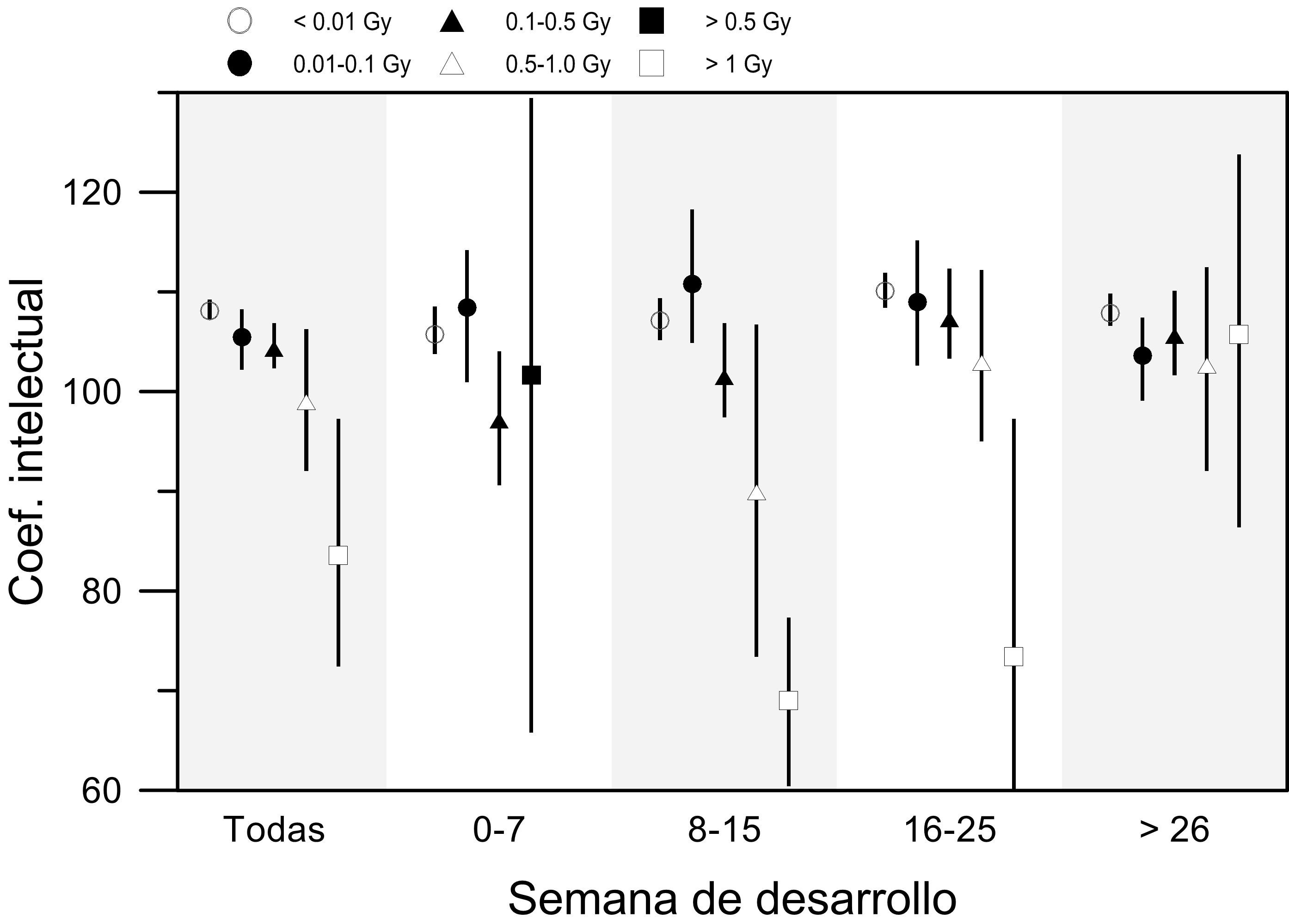
En números absolutos, el estudio, que compara 476 individuos irradiados con dosis superiores a los 5 mGy (hasta los casi 2000 mGy de aquellos más próximos al epicentro) y 1068 no irradiados, muestra en el primer grupo 21 casos de retraso mental severo (4.4 %) frente a 9 casos en el segundo grupo (0.8 %). La siguiente figura muestra como ese incremento de riesgo se reparte en función de la dosis y del estado de gestación en el que ocurrió la irradiación. A pesar de las incertidumbres tan grandes, debidas al reducido número de casos, la dependencia con la dosis señala claramente la relación causa-efecto.

Los descendientes de las víctimas: efectos hereditarios
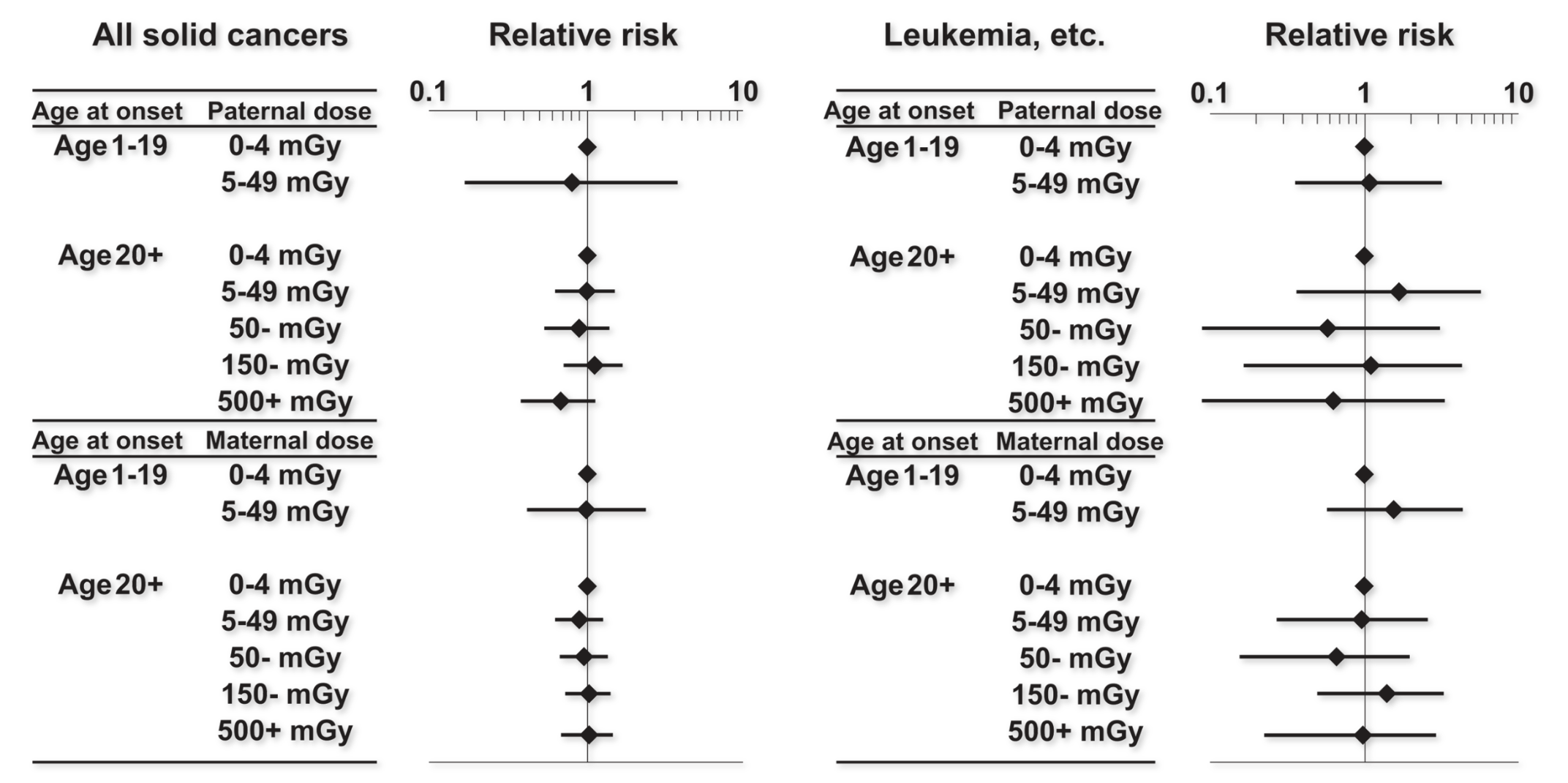
A pesar de todos los prejuicios existentes sobre el asunto, el seguimiento a largo plazo de 77000 descendientes nacidos en los nueve años posteriores al bombardeo, no muestra incremento de riesgo para cánceres sólidos, leucemias ni otras enfermedades. Tampoco se ha visto incrementada la incidencia de malformaciones, abortos, o muerte perinatal. No existe correlación ni con las dosis conjuntas de ambos progenitores ni con las dosis por separado. Información detallada sobre el estudio se recopila en este informe de libre acceso.
La existencia de estas secuelas hereditarias que traspasan generaciones, esta especie de «peste atómica» con la que los supervivientes fueron estigmatizados por sus propios compatriotas, no es más que un prejuicio, un mito. Una (otra) injusticia sufrida por aquellas víctimas y que provocó en ellas un miedo que les acompañaría en adelante, temiendo que esas radiaciones invisibles acabaran afectando a la salud de sus hijos, a los que veían crecer sanos.
Estos niños son hoy adultos, algunos han superado los 70 años. Aun así el estudio continúa registrando los posibles efectos sobre su salud y la incidencia de las diferentes patologías, sin que hasta la fecha se haya evidenciado ningún efecto significativo.
A modo de despedida
En los últimos años ha surgido una corriente crítica con el modelo lineal sin umbral, el cual ha reinado (y sigue haciéndolo) en el ámbito de la protección radiológica desde hace décadas. Se critica, también, la calidad de los datos que lo sustentan, no solo los de Hiroshima y Nagasaki (aunque estos principalmente).
El estudio de los efectos de la radiación realizado con el seguimiento de las víctimas de los bombardeos es sin duda un hito de la humanidad. Es el reverso luminoso de aquel lado tan oscuro de nuestra historia común. De aquel sufrimiento de las víctimas y el posterior esfuerzo de cientos o miles de investigadores ha surgido el modelo de gestión de riesgos con más fundamento científico de cuantos pueblan la actividad humana, y sigue siendo un ejemplo único. La complejidad de los datos y del trabajo de campo que requirió su recopilación, la dificultad de su ordenación y análisis, las complejas condiciones geopolíticas en las que el estudio se desarrolló, todo se une para que comprender su dimensión siga siendo tarea inaccesible incluso para los profesionales.
Espero que el post haya servido, al menos, para que tú también te sientas en deuda con aquellas personas cuyo sufrimiento sirvió, sin duda, para que otros, también tú, podamos disfrutar de forma segura de todas las aplicaciones útiles de las radiaciones ionizantes.






