Fraccionamiento espacial en radioterapia: un concepto poco conocido
Sumario:
A la hora de diseñar un tratamiento de radioterapia generalmente se considera que el volumen a tratar debe recibir una dosis de radiación lo más homogénea posible. Parece razonable, ya que si alguna parte recibe una dosis sensiblemente inferior a la prescrita por el oncólogo radioterapeuta podría comprometerse el control de la enfermedad en esa […]
A la hora de diseñar un tratamiento de radioterapia generalmente se considera que el volumen a tratar debe recibir una dosis de radiación lo más homogénea posible. Parece razonable, ya que si alguna parte recibe una dosis sensiblemente inferior a la prescrita por el oncólogo radioterapeuta podría comprometerse el control de la enfermedad en esa zona, y por el contrario, en los puntos donde la dosis sea mayor podría producirse un daño innecesariamente alto a los tejidos.
No obstante, esta idea está empezando a matizarse y parece que últimamente la homogeneidad no se considera tan esencial como antes. Las técnicas actuales permiten adaptar la zona de alta dosis a la forma del volumen blanco incluso cuando tiene concavidades que rodean órganos críticos que hay que proteger, pero esta conformación a menudo se consigue a costa de una menor homogeneidad. También son cada vez más habituales los tratamientos con boost integrado simultáneo, que implican necesariamente distribuciones de dosis no homogéneas, y tratamientos estereotáxicos para irradiar volúmenes pequeños, en los que el reducido tamaño de los campos de radiación y los efectos de penumbra hacen inevitable que la dosis en el centro del tumor sea mayor que en su periferia. Pero aunque ya no se dé tanta importancia a la homogeneidad de la dosis en el volumen blanco, en general sigue pareciendo una característica deseable.
Sin embargo existen técnicas que rompen con este principio y se basan en producir distribuciones de dosis extremadamente inhomogéneas: múltiples picos, islas o franjas estrechas de alta dosis dispuestas de forma regular y separadas por zonas que reciben una dosis mucho menor; es lo que se conoce como fraccionamiento espacial. Algunas de las técnicas que utilizan este concepto están en fase experimental y requieren instalaciones muy sofisticadas, otras ya se utilizan clínicamente y sus primeras versiones se remontan a la primera mitad del siglo XX. Pero ¿qué técnicas son esas?, ¿en qué casos pueden ser útiles?, ¿semejante herejía tiene algún fundamento teórico? Intentemos responder a estas preguntas…
Radioterapia en rejilla (grid therapy): regreso de una idea olvidada
Cuando no había aceleradores de electrones ni unidades de cobalto y la radioterapia externa se hacía con haces de rayos X de menor energía que sufrían una mayor atenuación en los tejidos, el factor que limitaba la dosis que se podía administrar a un tumor profundo era la reacción en piel a la entrada del haz, donde se producía la máxima deposición de energía. Pero los radioterapeutas sabían que el efecto de la radiación sobre la piel y otros tejidos no dependía sólo de la dosis, también de la extensión de la zona irradiada: cuanto más pequeña es ésta, mayor es la dosis que puede tolerar. Así, se les ocurrió dividir el haz de tratamiento en un conjunto de haces más estrechos separados por zonas no irradiadas, usando una pantalla de plomo perforada con agujeros de varios milímetros de diámetro que formaban una especie de rejilla. De este modo las zonas de piel que quedaban bajo los agujeros (las únicas que recibían radiación directa) podían tolerar dosis mayores y se recuperaban antes a partir de las zonas no irradiadas. Al mismo tiempo, la dispersión de la radiación en los tejidos hacía que la distribución de dosis en profundidad no fuera tan inhomogénea como en la superficie, y a pesar de que una parte considerable del tumor sólo recibía radiación dispersa, se conseguía un efecto terapéutico mayor que con radiación uniforme a dosis más bajas.
La técnica llegó a tener cierto predicamento pero cayó en desuso por considerarse innecesaria cuando llegaron los equipos de megavoltaje, capaces de generar haces mucho más penetrantes. Sin embargo, algunos centros vienen utilizando desde finales de los noventa una versión con megavoltaje para tratar tumores sólidos grandes (mayores de 8 cm), en los que las alternativas convencionales a menudo son poco eficaces o tienen mayores efectos secundarios. La práctica actual consiste en administrar una única sesión con fraccionamiento espacial alcanzando 15-20 Gy en los puntos de dosis máxima, complementada en la mayoría de los casos con unos 40 Gy de radioterapia fraccionada convencional. El tamaño de los haces o “beamlets” es del orden de 1 cm, aunque el patrón geométrico varía de unas implementaciones a otras. Según describen los usuarios de esta técnica, la alta dosis de la primera sesión se tolera bien por los tejidos sanos al estar fraccionada en pequeñas islas y acelera notablemente la reducción de volumen del tumor.
En la literatura esta modalidad de radioterapia recibe el nombre de “GRID therapy”. A algunos les gusta escribirlo así, con mayúsculas, como si fueran siglas, quizá para diferenciarlo de las versiones antiguas o para darle mayor solemnidad y que parezca una técnica comparable con otras como la IMRT o la IGRT, pero el autor de esta humilde entrada no ve ningún motivo para escribirlo de esa forma. Hasta ahora se ha utilizado principalmente en tumores avanzados con finalidad paliativa, pero también como parte de tratamientos curativos, por ejemplo para reducir el volumen del tumor con objeto de facilitar la cirugía.

Colimador utilizado en la técnica “Grid” (Buckey, 2010)

También se puede utilizar una secuencia de segmentos generados con el colimador multilámina (University of Maryland, Dept. Radiation Oncology)
Para obtener la matriz de beamlets algunos centros colocan en el cabezal del acelerador un bloque con agujeros que siguen la divergencia del haz y otros prefieren conseguir un efecto similar generando segmentos con el colimador multilámina, método más automático pero más lento. Generalmente se administra con un único campo de radiación, por lo que las zonas de alta dosis tienen forma de cilindros alargados que no sólo atraviesan el tumor sino también algunos tejidos sanos, pero están empezando a utilizarse métodos más sofisticados con equipos de arcoterapia modulada o radioterapia robotizada para conseguir que las islas de alta dosis tengan forma aproximadamente esférica y queden confinadas al tumor. A esta evolución de la técnica Grid algunos autores la llaman “lattice therapy”.

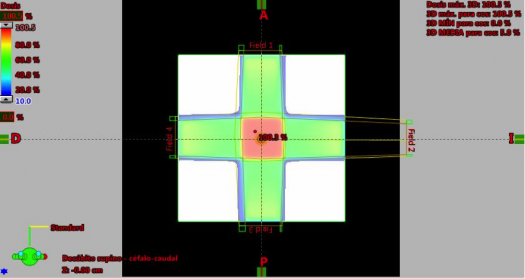
Distribuciones de dosis con la técnica Grid y con “lattice therapy” (Wu, 2010)
¿Y qué dice la radiobiología de todo esto? Varios artículos intentan dar soporte teórico a la técnica Grid en el marco de la radiobiología clásica mediante el modelo lineal-cuadrático estándar o una versión modificada para alta dosis por fracción. Para ello calculan el promedio espacial de la fracción de supervivencia para las células normales y tumorales, y bajo una serie de suposiciones concluyen que la técnica Grid es ventajosa frente a la radiación uniforme cuando la dosis por fracción es de al menos 15 Gy. Pero estos análisis no convencen a todos ni parece que puedan explicar completamente los resultados clínicos, y se piensa que en este tipo de tratamiento, al igual que en otros que utilizan alta dosis por fracción, pueden ser importantes algunos fenómenos que no se tienen en cuenta en la radiobiología clásica, como los efectos de vecindad inducidos por la radiación. También se ha especulado que la muerte celular inducida en algunas zonas del tumor por la alta dosis de la primera fracción facilitaría la reoxigenación del resto, mejorando la respuesta a las siguientes fracciones por el efecto oxígeno.
Varios cientos de pacientes se han tratado con la técnica Grid de megavoltaje desde los años noventa, la mayoría en Estados Unidos, sin que se haya publicado por el momento ningún ensayo aleatorizado que la compare con técnicas más convencionales. En nuestro centro hemos tenido varios casos que quizá podrían haberse beneficiado de esta técnica y existe interés por parte de algunos oncólogos radioterapeutas, lo que nos ha llevado a trabajar en una implementación propia (todavía no probada clínicamente) con medios relativamente modestos. Veremos en qué queda la cosa.
Minihaces y microhaces, llevando el concepto al límite.
Aunque el aumento de la dosis de tolerancia al disminuir el volumen irradiado ocurre en mayor o menor medida en la mayoría de los tejidos (si no en todos), los haces de la técnica Grid siguen siendo muy grandes para utilizarlos sobre el sistema nervioso central y otros órganos críticos. Sin embargo se sabe por experimentos con animales que cuando la anchura del haz se reduce a tamaños microscópicos es posible administrar en una sola fracción dosis pico de cientos de grays con buena tolerancia de los tejidos sanos. Ésta es la base de la radioterapia con microhaces, una técnica en fase experimental que utiliza estrechas franjas paralelas de rayos X con un espesor de 25-50 micras separadas entre sí una distancia del orden de 0,2 mm. En los ensayos con roedores se observa que además de ser bien tolerada por los tejidos sanos, este tipo de irradiación es muy efectiva en el tratamiento de gliomas y otros tumores radiorresistentes. La explicación no se sabe pero se barajan dos hipótesis: la distinta sensibilidad de las células sanas y cancerosas a los efectos “bystander” y la distinta capacidad de los tejidos sanos y los tumores para reparar los daños producidos por la radiación en la microvasculatura.
Un inconveniente de esta técnica es que cualquier mínimo movimiento difumina la distribución de dosis y elimina el patrón de fraccionamiento espacial. Para evitarlo se necesitan disparos muy cortos con una tasa de dosis extremadamente alta, algo que por ahora sólo se puede conseguir en complejas instalaciones científicas mediante radiación sincrotrón (en los sincrotrones de tercera generación se alcanzan tasas de hasta 20 kGy/s). Además, en este tipo de fuentes la energía media de los rayos X en es bastante baja, del orden de 100 keV, que no parece adecuada para tratar tumores profundos. Aún así, algunos investigadores piensan que podría llegar a utilizarse para tratar tumores cerebrales pediátricos y que permitiría reducir las secuelas neurológicas que la radioterapia actual produce en estos casos. La atenuación de la radiación en los tejidos podría compensarse usando un agente de contraste para aumentar la absorción de energía en el tumor por efecto fotoeléctrico.
Otros grupos están dirigiendo sus investigaciones hacia radioterapia con minihaces de aproximadamente 0,6 mm de espesor y una separación de centro a centro cercana a 1,2 mm. Esta técnica conserva parte de la ventaja radiobiológica de los microhaces pero no es tan extremadamente sensible al movimiento, y podría implementarse con fuentes de rayos X más compactas y económicas y haces de mayor energía, más adecuados en principio para el tratamiento de tumores profundos. No obstante, no parece posible implementar esta modalidad en aceleradores lineales convencionales con haces de megavoltaje por la dificultad de conseguir un patrón de franjas de irradiación tan fino con el suficiente grado de modulación, además de por los tiempos de irradiación prohibitivamente altos que se necesitarían para administrar dosis tan elevadas en haces tan estrechos.
Me parece curioso que un concepto de radioterapia que fue abandonado en su día por considerarlo obsoleto, vuelva a encontrar aplicación en algunos de los enfoques más novedosos y parezca cobrar más sentido a la luz de los descubrimientos modernos de la radiobiología.
Para finalizar quiero agradecer a Yolanda Prezado, radiofísica española responsable de un grupo de investigación en el CNRS francés, la información que me ha facilitado sobre la radioterapia con microhaces y minihaces.